Carburo de silicio frente a silicio: Estudio comparativo de semiconductores en aplicaciones de alta temperatura
1 Introducción
Con la amplia aplicación de los semiconductores en diversos aspectos de la producción y la vida, los requisitos de rendimiento de los materiales semiconductores en diferentes escenarios de uso son cada vez más diversos. En muchos entornos de aplicación, los materiales semiconductores deben trabajar a altas temperaturas, lo que exige una elevada estabilidad térmica, estabilidad eléctrica y densidad de potencia de los materiales semiconductores. En virtud de estos requisitos, las obleas de carburo de silicio (SiC) y silicio (Si ) han recibido atención como materiales semiconductores con estructura y propiedades estables y buena estabilidad térmica. La estructura de diamante de estos dos cristales atómicos los hace extremadamente estables térmicamente, y pueden asumir más funciones semiconductoras en entornos de alta temperatura. En este artículo, analizaremos las diferencias de rendimiento y las razones de su desempeño en escenarios de aplicación de semiconductores a alta temperatura desde la perspectiva de la estructura cristalina y las propiedades fisicoquímicas, y proporcionaremos referencias para su elección en combinación con el proceso de preparación y el coste.
2 Estructura cristalina y propiedades del carburo de silicio y la oblea de silicio
2.1 Estructura cristalina y propiedades del carburo de silicio
De acuerdo con la estructura cristalina, el carburo de silicio puede dividirse en carburo de silicio α hexagonal y carburo de silicio β cúbico. El carburo de silicio α (α-SiC) es el tipo policristalino más común, y de acuerdo con la disposición de los átomos, se divide en 4H-SiC y 6H-SiC, y en la estructura cristalina 4H-SiC, los átomos de silicio y los átomos de carbono están dispuestos en capas alternas, lo que forma la estructura de red cristalina hexagonal; mientras que en el 6H-SiC, forma la estructura de red cristalina hexagonal y tetragonal alterna. La figura 1 ilustra la disposición atómica de estas dos estructuras cristalinas.
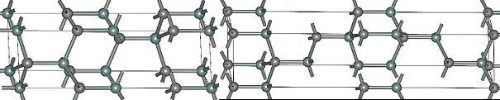
Fig.1 Estructura cristalina de 4H-SiC(izquierda) y 6H-SiC(derecha)
En el caso del α-SiC, algunas de las propiedades del 4H-SiC y del 6H-SiC son ligeramente diferentes debido a pequeñas diferencias en sus estructuras reticulares. El 4H-SiC tiene una gran tolerancia al desajuste de la red, que caracteriza la capacidad del cristal para mantener un cierto grado de estabilidad y calidad cristalina incluso cuando hay una coincidencia imperfecta entre las disposiciones atómicas en la red y es un parámetro importante para describir la plasticidad y la estabilidad del material cristalino bajo la acción de la tensión. Es un parámetro importante para describir la plasticidad y la estabilidad de los materiales cristalinos bajo la acción de la tensión. La combinación de una mayor tolerancia al desajuste de la red con una mayor intensidad de campo de ruptura y una mejor conductividad eléctrica se traduce en una mayor estabilidad y fiabilidad de los dispositivos de 4H-SiC, que ofrecen un buen rendimiento en electrónica y optoelectrónica de alta potencia. En cambio, el 6H-SiC tiene mayor movilidad de electrones y menor sección transversal de captura de electrones, lo que confiere al 6H-SiC mejores propiedades de transporte de portadores, incluida la movilidad y la vida útil.
El carburo de silicio β (β-SiC) puede representarse como 3C-SiC según la disposición atómica, en la que cada átomo de silicio está rodeado por cuatro átomos de carbono y cuatro átomos de silicio vecinos en la estructura de red cúbica. La figura 2 muestra la estructura de su disposición atómica.
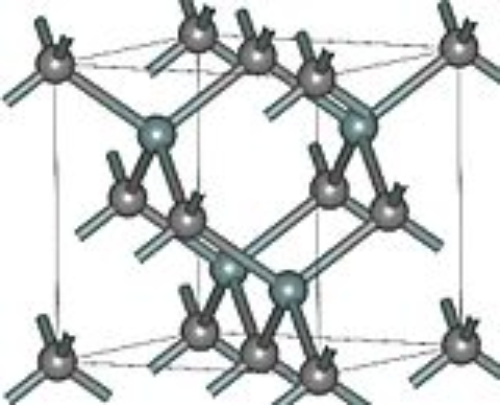
Fig.2 Estructura cristalina del 3C-SiC
En comparación con el β-SiC, los α-SiC ofrecen una mayor rentabilidad y fiabilidad de los dispositivos, ya que sus estructuras cristalinas presentan una mayor estabilidad, menores concentraciones de impurezas y menores densidades de defectos, lo que les permite funcionar en condiciones de altas temperaturas, alta potencia y alto voltaje. En cuanto al 3C-SiC, su estructura cristalina le permite tener la mayor velocidad teórica de electrones, pero es susceptible a las impurezas, lo que da lugar a trazas de corrosión por impurezas. El 3C-SiC tiene una alta movilidad de electrones y velocidad de deriva de saturación de electrones, así como una baja concentración de impurezas y corrientes de fuga, lo que permite su uso en electrónica de alta potencia, dispositivos de RF, etc., pero debido a la diferencia en su estructura de red cristalina y los materiales de sustrato de silicio, por lo que no es adecuado para la fabricación de circuitos integrados. Diferentes estructuras cristalinas de SiC propiedades físicas y químicas específicas y la estructura cristalina de los parámetros pertinentes se pueden ver en la Tabla 1.
Tabla 1 Propiedades de los cristales de SiC con diferentes estructuras cristalinas
|
Tipo |
3C |
4H |
6H |
|
Estructura cristalina |
Estructura de tipo esfalerita (sistema cristalino cúbico) |
Sistema Cristalino Hexagonal |
Sistema cristalino hexagonal |
|
Grupo espacial |
T2d-F43m |
C46v-P63mc |
C46v-P63mc |
|
Símbolo de Pearson |
cF8 |
hP8 |
hP12 |
|
Parámetros celulares(Å) |
4.3596 |
3.0730; 10.053 |
3.0810; 15.12 |
|
Densidad(G/Cm3) |
3.21 |
3.21 |
3.21 |
|
Bandgap de referencia(eV) |
2.36 |
3.23 |
3.05 |
|
Módulo de masa(GPa) |
250 |
220 |
220 |
|
Conductividad térmica [W/(M-K) |
360 |
370 |
490 |
2.2 Estructura cristalina y propiedades del silicio
Los cristales de silicio tienen una estructura típica de diamante, con átomos de silicio dispuestos equidistantemente para formar una red cúbica, y cada átomo de silicio conectado a los cuatro átomos de silicio circundantes mediante enlaces covalentes para formar una estructura orto-tetraédrica extremadamente estable, que confiere a los monómeros de silicio un punto de fusión (1414°C) y una estabilidad térmica elevados. La figura 3 es una representación esquemática de la estructura de un cristal de silicio.
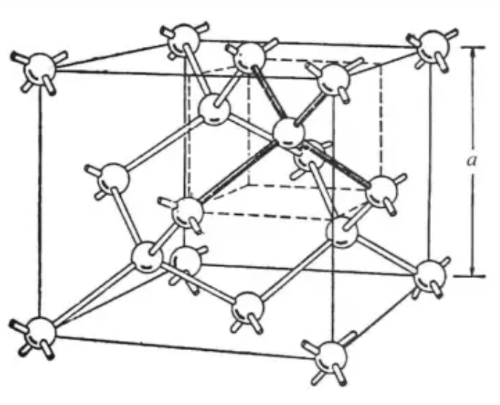
Fig.3 Estructura cristalina del Si
Cada átomo de silicio de un cristal de silicio está conectado a cuatro átomos de silicio circundantes mediante enlaces covalentes, formando una estructura cristalina estable. Esto hace que el silicio sea química y térmicamente estable, con un punto de fusión de unos 1414 grados Celsius. El silicio también tiene una alta conductividad térmica de entre 1,5 y 1,7 vatios por metro-kelvin (W/m-K), lo que lo hace importante para la disipación del calor y las aplicaciones de gestión térmica. El silicio es un semiconductor de banda prohibida indirecta con un ancho de banda de aproximadamente 1,1 electronvoltios (eV). A temperatura ambiente, el silicio se comporta como un aislante, pero cuando se excita (por ejemplo, por un aumento de la temperatura o la aplicación de un campo eléctrico), los electrones pueden saltar a la banda de conducción, convirtiéndolo en un semiconductor. En los cristales de silicio puro, la concentración de electrones y huecos es muy baja, por lo que se comporta como un aislante. Sin embargo, mediante el dopaje o la aplicación de un campo eléctrico, se pueden introducir portadores libres adicionales, haciendo que el silicio muestre la conductividad de un semiconductor o conductor.
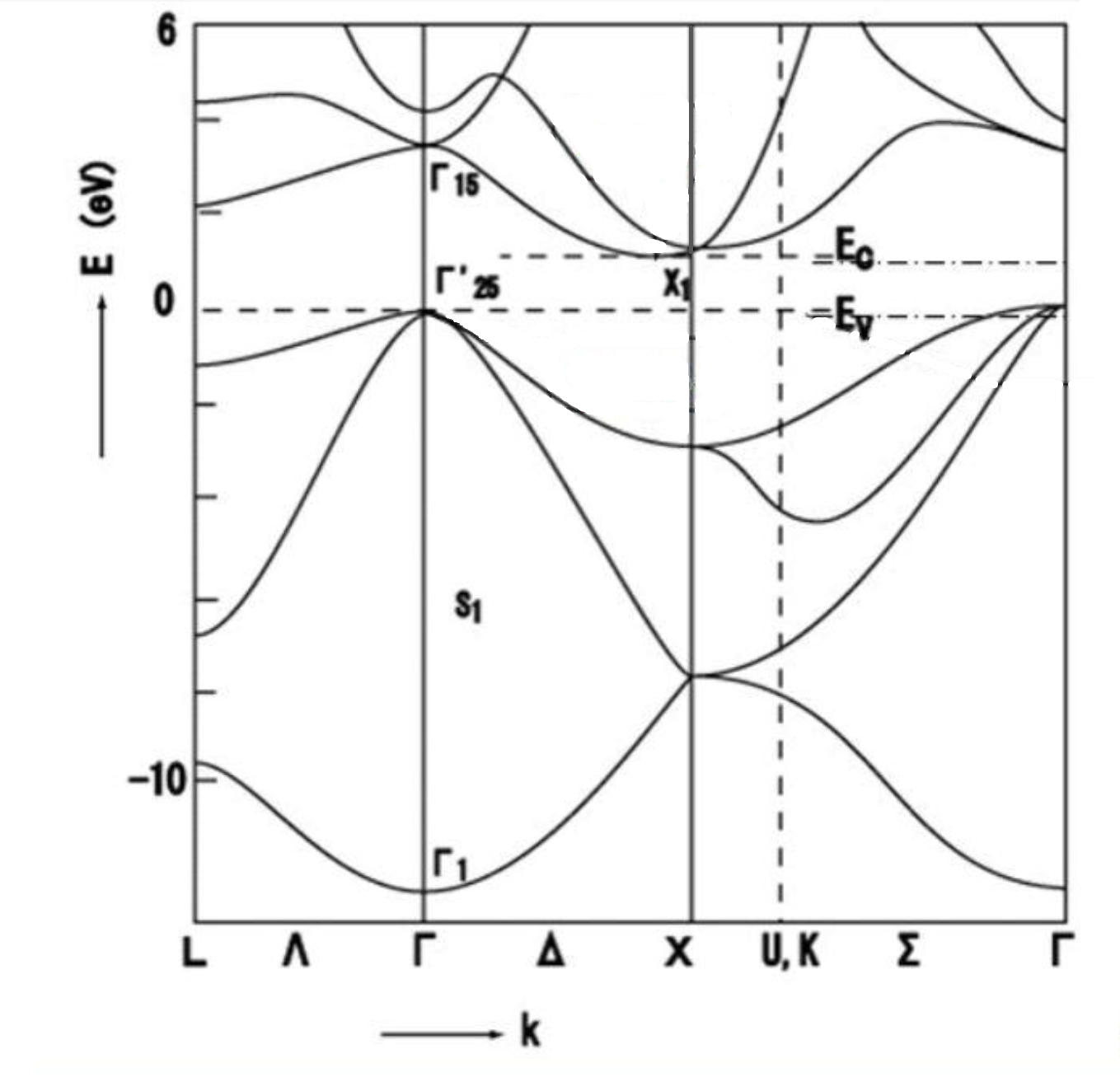
Fig.4 Diagrama de la estructura de bandas de energía de un cristal de silicio
3 Por qué el SiC y el Si son mejores que otros materiales semiconductores
3.1 Desafíos para los materiales semiconductores en entornos de alta temperatura
A altas temperaturas, los materiales son susceptibles de sufrir tensiones térmicas y dilataciones térmicas que alteran la estructura cristalina y degradan sus propiedades. Para los materiales semiconductores, especialmente los de silicio, la estabilidad térmica es crítica. La estructura cristalina no sólo afecta al índice de rendimiento del dispositivo, sino que también puede tener un impacto directo en el funcionamiento y la seguridad de todo el proceso. Al mismo tiempo, las propiedades eléctricas de los materiales semiconductores son propensas a cambiar en entornos de alta temperatura, por ejemplo, la conductividad, la concentración de portadores, etc. pueden verse afectadas por la temperatura y cambiar, lo que puede provocar una disminución del rendimiento de los dispositivos electrónicos o un fallo. Además, los materiales semiconductores en entornos de alta temperatura son propensos a reacciones químicas con el oxígeno, vapor de agua, etc. en el entorno circundante, lo que resulta en la oxidación de la superficie del material, la corrosión, o la difusión de impurezas en el material, y otros fenómenos, que afectan a la estabilidad y la vida útil del dispositivo. El calor generado en el interior del dispositivo que trabaja en un entorno de alta temperatura también puede hacer que la temperatura aumente de nuevo, afectando así al rendimiento y la estabilidad del dispositivo. Por lo tanto, unos buenos sistemas de conducción térmica y disipación del calor son fundamentales para los dispositivos semiconductores en entornos de alta temperatura.
3.2 Ventajas y desventajas del carburo de silicio y el silicio
3.2.1 Propiedades térmicas
El Si tiene un punto de fusión de unos 1414 grados Celsius y el SiC tiene un punto de fusión de unos 2700 grados Celsius. La conductividad térmica del silicio es de aproximadamente 1,5-1,7 vatios por metro-kelvin (W/m-K). El SiC tiene una conductividad térmica mayor, normalmente entre 3 y 4,9 vatios por metro-kelvin (W/m-K), dependiendo de la temperatura y la estructura cristalina. Como muestra la figura 5, la conductividad térmica del carburo de silicio es tres veces superior a la del silicio. Desde un punto de vista global de la capacidad de soportar entornos de alta temperatura, el carburo de silicio puede soportar temperaturas más altas que el silicio y tiene un rendimiento de disipación térmica más excelente, lo que puede priorizarse en el uso de requisitos de temperatura extremadamente alta.
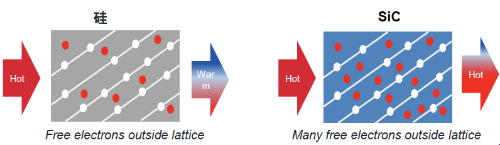
Fig.5 El carburo de silicio tiene una conductividad térmica 3 veces superior a la del silicio
3.2.2 Propiedades fotoeléctricas
El SiC es un semiconductor de banda ancha con una anchura de banda prohibida de 2,2 a 3,3 electronvoltios (eV). El Si es un semiconductor de banda estrecha con una anchura de banda prohibida menor, de aproximadamente 1,1 electronvoltios (eV). La anchura de la banda prohibida determina las propiedades conductoras del material. Los materiales con un bandgap pequeño suelen comportarse como buenos conductores o semiconductores porque los electrones pueden saltar a la banda de conducción con relativa facilidad y participar en el comportamiento conductor. Por el contrario, los materiales con mayores huecos de banda suelen comportarse como aislantes porque los electrones necesitan energías más altas para saltar a la banda de conducción, lo que da lugar a materiales con pocos portadores libres a temperatura ambiente. La anchura del bandgap también determina las propiedades ópticas del material, como la absorción, emisión y transmisión de la luz. Los materiales con bandgaps más pequeños suelen presentar buenas propiedades de absorción de la luz porque pueden absorber más fotones. Por el contrario, los materiales con bandgaps mayores suelen ser transparentes o translúcidos porque sólo pueden absorber fotones con energías superiores a la anchura del bandgap. Estos diferentes rendimientos de las propiedades también determinan que el SiC y el Si se apliquen en diferentes escenarios de uso.
3.2.3 Propiedades mecánicas y estabilidad química
La dureza Mohs del SiC es de aproximadamente 9-9,5, cercana a la dureza del diamante, mientras que la dureza Mohs del Si es de aproximadamente 7, ligeramente inferior a la del SiC. La elevada dureza del SiC le confiere una buena resistencia a la abrasión y al rayado, por lo que resulta adecuado para la fabricación de dispositivos que requieren resistencia a la abrasión. Al mismo tiempo, la resistencia del SiC suele ser mayor que la del Si. El SiC tiene una excelente resistencia a la flexión y a la tracción y puede soportar mayores tensiones sin deformarse ni romperse. El SiC tiene una buena estabilidad química a temperatura ambiente y no es fácilmente atacado por ácidos, álcalis y disolventes, mientras que el Si es atacado por algunos agentes oxidantes fuertes y ácidos fuertes.
4 Diferentes escenarios de aplicación para el carburo de silicio y el silicio
Teniendo en cuenta las distintas propiedades del SiC y el Si derivadas de sus estructuras cristalinas, es evidente cómo sus aplicaciones se adaptan a sus puntos fuertes.
El SiC posee una estabilidad térmica y una resistencia a las altas temperaturas excepcionales, lo que lo hace ideal para fabricar dispositivos electrónicos que funcionan en condiciones de calor extremo. Entre sus aplicaciones se encuentran los dispositivos de potencia y de radiofrecuencia, entre otros. Su sólido rendimiento en entornos de altas temperaturas abre posibilidades para satisfacer las demandas de sectores como la electrónica de potencia, las comunicaciones por RF y la electrónica del automóvil. Además, la mayor anchura de la banda prohibida del SiC se traduce en mayores tensiones de ruptura y menor resistencia a la conexión, lo que lo hace especialmente adecuado para la fabricación de dispositivos de alta potencia, como MOSFET y diodos de potencia.

Por otro lado, el Si es uno de los materiales semiconductores más utilizados en dispositivos electrónicos convencionales como transistores, circuitos integrados y células solares. Es la piedra angular de la microelectrónica y se beneficia de tecnologías de preparación y métodos de procesamiento maduros que permiten altos niveles de integración y miniaturización. La versatilidad del Si se extiende a aplicaciones optoelectrónicas como LED, láseres, fotodetectores y células solares, aprovechando sus excelentes propiedades fotovoltaicas y su eficiencia de conversión fotoeléctrica.
5 Conclusiones
En comparación con el silicio, el carburo de silicio tiende a tener una gama más amplia de aplicaciones en escenarios de temperaturas más elevadas, pero debido a su proceso de preparación y a la pureza del producto acabado obtenido, las obleas de silicio siguen siendo la opción más utilizada en los casos en que los requisitos de temperatura ambiente son relativamente bajos. Stanford Advanced Materials suministra obleas de carburo de silicio y obleas de silicio de alta calidad para sus diversas utilizaciones.
Lectura relacionada:
Elementos calefactores: Disiliciuro de Molibdeno vs Carburo de Silicio
Estudio de caso: Placas de carburo de silicio para soluciones avanzadas de blindaje
El gran avance del sustrato de carburo de silicio en la industria LED
Referencia:
[1]Fenglin G ,Chen S ,Xiufang C , et al. Modulación de la forma debida a la diferencia de daños subsuperficiales en obleas de 4H-SiC de tipo N durante el lapeado y pulido[J]. Ciencia de los materiales en el procesamiento de semiconductores,2022,152.

 Bares
Bares
 Cuentas y esferas
Cuentas y esferas
 Tornillos y tuercas
Tornillos y tuercas
 Crisoles
Crisoles
 Discos
Discos
 Fibras y tejidos
Fibras y tejidos
 Películas
Películas
 Escama
Escama
 Espumas
Espumas
 Folio
Folio
 Gránulos
Gránulos
 Panales
Panales
 Tinta
Tinta
 Laminado
Laminado
 Bultos
Bultos
 Mallas
Mallas
 Película metalizada
Película metalizada
 Placa
Placa
 Polvos
Polvos
 Varilla
Varilla
 Hojas
Hojas
 Cristales individuales
Cristales individuales
 Blanco para sputtering
Blanco para sputtering
 Tubos
Tubos
 Lavadora
Lavadora
 Cables
Cables
 Conversores y calculadoras
Conversores y calculadoras
 Chin Trento
Chin Trento



